Перевод: berenzorn
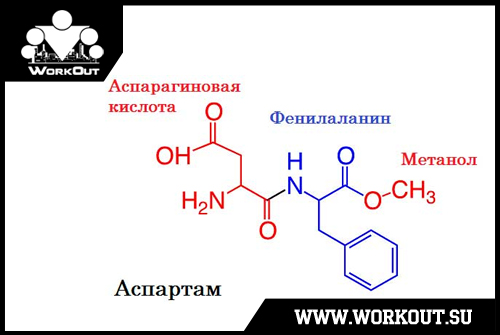
А вы знали, что аспартам (содержится в большинстве газированных напитков двух известных компаний) был дважды запрещен американским Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA)? Как же этот продукт стал теперь легальным?
Споры о том, опасен аспартам или нет, длятся долгое время. С одной стороны мы имеем медицинские доказательства, что должны избегать его использования, с другой стороны мы полагаемся на одобрение от FDA, означающее, что аспартам безопасен. Принимая во внимание, что многие продолжают доверять этой организации, я думаю, что мы сами должны заглянуть в историю аспартама, чтобы понять, как же получилось, что он признан FDA безопасным.
Всё началось в середине 60-х годов с компании G.D. Searle. Один из химиков случайно создал аспартам в процессе поиска лекарства для лечения язвы желудка. Компания решила запустить процесс тестирования аспартама, который в конечном итоге привел к одобрению его FDA. Через некоторое время начали проявляться серьёзные побочные эффекты и компания Searle попала под огонь критики. Выяснилось, что процесс тестирования аспартама был одним из худших, которые когда-либо видели исследователи и продукт на самом деле небезопасен. FDA возбудило уголовное расследование, которое было запущено в 1977 году. В 1980 году, после исследования подсластителя тремя независимыми исследователями, FDA запретило аспартам к использованию. Было установлено, что среди главных воздействий на здоровье человека была вероятность возникновения опухоли головного мозга. В то время было ясно, что аспартам запрещен к использованию в питании, но это продлилось недолго.
В начале 1981 директор компании Searle Дональд Рамсфельд (бывший Министр Обороны США, сюрприииз) пообещал задействовать свои связи, чтобы вещество разрешили. 21 января 1981 года, через день после инаугурации нового президента Рональда Рейгана, компания Searle приняла шаги для возвращения аспартама в список разрешённых FDA. Назначенный Рейганом новый председатель FDA Артур Халл собрал научную комиссию из пяти человек для рассмотрения этого вопроса. Много времени это не заняло, комиссия тремя голосами против двух высказалась за сохранение запрета на аспартам. Тогда Халл решил назначить в комиссию шестого человека, который уравнял новое голосование, 3 против 3. После этого Халл решил сам решить ничейную ситуацию и лично разрешил аспартам к использованию. Позже он покинул FDA из-за обвинений в некорректности и занял должность в Burson-Marsteller, компании, ответственной за связи с общественностью для Searle и Monsanto. C тех пор он никогда не говорил публично об аспартаме.
Здесь мы понимаем, что все доводы, связанные с безопасностью аспартама, крайне шаткие. Прошедший через запрет к использованию и незаконную процедуру разрешения, он не должен использоваться сегодня. Удивляет, как много коррупции и денег связано с такими именами, как Рамсфельд, Рейган и Халл. В 1985 году компания Monsanto решила выкупить патент на аспартам у G.D. Searle. Мы помним, что Халл теперь имел отношение к Monsanto. Компания, похоже, была не слишком озабочена прошлыми проблемами с веществом и его негативным имиджем. Я лично считаю это комичным, что продукция Monsanto запрещена во многих странах, и из всех компаний, которые могли бы купить этот патент, они подошли как нельзя лучше - как чемпионы по производству невероятно опасных и непроверенных продуктов, предварительно убедившись, что он останется на рынке.
С тех пор аспартам много раз был под ударами учёных, докторов, химиков и простых покупателей, твердивших о его опасности и нейротоксическом воздействии. Были сделаны горы объемных исследований, которые показывали, что аспартам может быть причиной более 90 серьёзных заболеваний, среди которых рак, лейкемия, мигрень и эпилепсия.
Оригинал: http://www.collective-evolution.com/2013/01/19/the-shocking-story-of-how-aspartame-became-legal/

А вы знали, что аспартам (содержится в большинстве газированных напитков двух известных компаний) был дважды запрещен американским Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA)? Как же этот продукт стал теперь легальным?
Споры о том, опасен аспартам или нет, длятся долгое время. С одной стороны мы имеем медицинские доказательства, что должны избегать его использования, с другой стороны мы полагаемся на одобрение от FDA, означающее, что аспартам безопасен. Принимая во внимание, что многие продолжают доверять этой организации, я думаю, что мы сами должны заглянуть в историю аспартама, чтобы понять, как же получилось, что он признан FDA безопасным.
Всё началось в середине 60-х годов с компании G.D. Searle. Один из химиков случайно создал аспартам в процессе поиска лекарства для лечения язвы желудка. Компания решила запустить процесс тестирования аспартама, который в конечном итоге привел к одобрению его FDA. Через некоторое время начали проявляться серьёзные побочные эффекты и компания Searle попала под огонь критики. Выяснилось, что процесс тестирования аспартама был одним из худших, которые когда-либо видели исследователи и продукт на самом деле небезопасен. FDA возбудило уголовное расследование, которое было запущено в 1977 году. В 1980 году, после исследования подсластителя тремя независимыми исследователями, FDA запретило аспартам к использованию. Было установлено, что среди главных воздействий на здоровье человека была вероятность возникновения опухоли головного мозга. В то время было ясно, что аспартам запрещен к использованию в питании, но это продлилось недолго.
В начале 1981 директор компании Searle Дональд Рамсфельд (бывший Министр Обороны США, сюрприииз) пообещал задействовать свои связи, чтобы вещество разрешили. 21 января 1981 года, через день после инаугурации нового президента Рональда Рейгана, компания Searle приняла шаги для возвращения аспартама в список разрешённых FDA. Назначенный Рейганом новый председатель FDA Артур Халл собрал научную комиссию из пяти человек для рассмотрения этого вопроса. Много времени это не заняло, комиссия тремя голосами против двух высказалась за сохранение запрета на аспартам. Тогда Халл решил назначить в комиссию шестого человека, который уравнял новое голосование, 3 против 3. После этого Халл решил сам решить ничейную ситуацию и лично разрешил аспартам к использованию. Позже он покинул FDA из-за обвинений в некорректности и занял должность в Burson-Marsteller, компании, ответственной за связи с общественностью для Searle и Monsanto. C тех пор он никогда не говорил публично об аспартаме.
Здесь мы понимаем, что все доводы, связанные с безопасностью аспартама, крайне шаткие. Прошедший через запрет к использованию и незаконную процедуру разрешения, он не должен использоваться сегодня. Удивляет, как много коррупции и денег связано с такими именами, как Рамсфельд, Рейган и Халл. В 1985 году компания Monsanto решила выкупить патент на аспартам у G.D. Searle. Мы помним, что Халл теперь имел отношение к Monsanto. Компания, похоже, была не слишком озабочена прошлыми проблемами с веществом и его негативным имиджем. Я лично считаю это комичным, что продукция Monsanto запрещена во многих странах, и из всех компаний, которые могли бы купить этот патент, они подошли как нельзя лучше - как чемпионы по производству невероятно опасных и непроверенных продуктов, предварительно убедившись, что он останется на рынке.
С тех пор аспартам много раз был под ударами учёных, докторов, химиков и простых покупателей, твердивших о его опасности и нейротоксическом воздействии. Были сделаны горы объемных исследований, которые показывали, что аспартам может быть причиной более 90 серьёзных заболеваний, среди которых рак, лейкемия, мигрень и эпилепсия.
История аспартама
Name:>
Декабрь 1965 – Работая над лекарством от язвы желудка, Джеймс Шлаттер, химик компании G.D. Searle, случайно открыл аспартам, вещество, которое в 180 раз слаще сахара и при этом не содержит калорий.
Весна 1967 - G.D. Searle начало тестирование аспартама на безопасность, требующееся для признания его годным к употреблению в пищу.
Осень 1967 – доктор Гарольд Вайсман, биохимик Университета Висконсина, по заказу G.D. Searle провел тесты аспартама на молодых обезьянах. Из семи обезьян, которые принимали аспартам, растворенный в молоке, одна умерла и ещё пять заболели тяжёлой формой эпилепсии.
Ноябрь 1970 – Цикламат, широко распространенный низкокалорийный синтетический подсластитель, был выкинут с рынка после того, как некоторые ученые связали его с возникновением рака. Вопросы возникли так же к Сахарину, второму синтетическому подсластителю на рынке, открывая аспартаму широкое поле для деятельности.
18 декабря 1970 – руководство G.D. Searle рассказало в своей стратегии о предчувствиях, что FDA «думает в положительном ключе об аспартаме». Внутренние документы описывали психологическую тактику, которая должна использовать компания, чтобы «FDA подсознательно прониклось духом сотрудничества и у руководства Управления вошло в привычку говорить «да».
Весна 1971 – нейробиолог Джон Олни (чьи работы о глутамате натрия ранее привели к удалению вещества из детского питания) информировал G.D. Searle, что аспарагиновая кислота, один из ингредиентов аспартама, в его опытах вызвала разрушение головного мозга у мышей. Один из сотрудников компании подтвердил результаты Олни в похожем исследовании.
Февраль 1973 – потратив десятки миллионов долларов на проведение тестирования, G.D. Searle подала заявку FDA на разрешение и приложила более сотни положительных исследований, доказывающих безопасность аспартама.
5 марта 1973 – один из ведущих ученых FDA в аннотации к тестам аспартама заметила, что приведенной G.D. Searle информации недостаточно, чтобы оценить потенциальную токсичность аспартама, и нужны дальнейшие клинические испытания.
Май 1974 – адвокат Джим Тернер (защитник прав потребителей, сыгравший роль в выведении Цикламата с рынка) встретился с представителями G.D. Searle по поводу исследования Джоном Олни аспарагиновой кислоты в 1971 году.
26 июля 1974 – FDA разрешило аспартам к ограниченному использованию в сухом питании.
Август 1974 – Джим Тернер и Джон Олни предоставили доказательства против аспартама.
24 марта 1976 – петиция Тернера и Олни возбудила расследование FDA лабораторной практики производителя аспартама G.D. Searle. Комиссия обнаружила в процедурах G.D. Searle большое количество несоответствий и манипулирования данными.
10 января 1977 – FDA сделало официальный запрос прокурору штата начать расследование против G.D. Searle за намеренное искажение данных, «сокрытие существенных фактов и дачу ложных показаний» в тестах безопасности аспартама. В первый раз в своей истории Управление по санитарному надзору возбудило уголовное дело на производителя.
26 января 1977 – во время расследования дела компания Sidley & Austin, юридическая фирма, представлявшая интересы G.D. Searle, начала переговоры с Самуэлем Скиннером, прокурором, ведущим расследование.
8 марта 1977 - G.D. Searle наняла на должность генерального директора видного вашингтонского политика Дональда Рамсфельда, который должен был помочь компании выйти из тяжелой ситуации. Бывший сенатор и Министр Обороны в администрации Форда, Рамсфельд привел с собой в высшее руководство компании нескольких своих помощников.
1 июля 1977 – Самуэль Скиннер, расследовавший дело G.D. Searle, покинул своё кресло и перешел на работу в Sidley & Austin.
1 августа 1977 – выпущено заключение Бресслера, составленное комиссией FDA под руководством Джерома Бресслера. Комиссия нашла, что во время тестирования 98 из 196 животных умерли и не были вовремя вскрыты, а некоторые тела ждали своей очереди более года. Также была отмечена масса других нарушений, например крыса по документам была живой, потом мертвой, потом снова живой и снова мертвой. У животных находили маточные полипы и злокачественные образования яичников, но это никак не отражалось в официальных отчетах G.D. Searle.
8 декабря 1977 – отставка прокурора Скиннера так затянуло следствие, что временное ограничение на выпуск аспартама потеряло свою силу. Уголовное дело было закрыто.
1 июня 1979 – FDA создает Общественный Совет по расследованию вопросов, связанных с безопасностью NutraSweet, торговой марки аспартама.
30 сентября 1980 – общественный совет постановил запретить NutraSweet к употреблению до проведения дальнейших исследований, связанных с опухолями мозга у подопытных животных. Совет утвердил, что не было предоставлено достаточных доказательств, что аспартам безопасен для использования в качестве пищевой добавки.
Январь 1981 – Дональд Рамсфельд, гендиректор G. D. Searle, заявил, что сделает всё возможное для разрешения аспартама к использованию в течение года, а также, что он будет использовать свой политический вес в Вашингтоне, а не научные средства, чтобы убедиться в принятии разрешения.
21 января 1981 – инаугурация Рональда Рейгана в качестве президента США. Команда Рейгана, в которую входит Дональд Рамсфельд, ставит на должность руководителя FDA Артура Халла Хейса.
Март 1981 – собрана комиссия FDA для рассмотрения вопросов, поднятых Общественным Советом по расследованиям.
19 мая 1981 – три из шести штатных биологов FDA, ответственных за рассмотрение случаев опухолей головного мозга животных, выступили против нового разрешения NutraSweet, основываясь на записях, что тестирование Searle было некачественным и недостаточным для признания аспартама безопасным.
15 июля 1981 – одним из своих первых приказов Артур Хейс, новый председатель FDA, действуя против указаний Общественного Совета и игнорируя рекомендации его собственной команды биологов разрешает NutraSweet к применению в сухом питании. Хейс сказал, что для предполагаемого применения аспартам доказал свою безопасность и лишь немногие вещества выдержали такое детальное тестирование и такое пристальное внимание.
15 октября 1982 – FDA анонсировало, что Searle прислало петицию о разрешении применения аспартама в газированных напитках и других жидкостях.
1 июля 1983 – Ассоциация Производителей Газированных Напитков (NSDA) попросила FDA отложить разрешение аспартама до проведения новых тестов, поскольку аспартам очень нестабилен в жидкой форме. Аспартам в жидкой форме при температуре выше 30 градусов Цельсия распадается на DKP (дикетопиперазины) и формальдегид – оба известные канцерогены.
8 июля 1983 - NSDA разработала возражения против принятия разрешения на использование аспартама в газированных напитках и сиропах и подала запрос на слушания по своим возражениям. NSDA сказала, что Searle не предоставила достаточно доказательств, что аспартам и продукты его разложения безопасны для использования в газированных напитках.
8 августа 1983 – защитник прав потребителей Джим Тернер из Национального Института Питания и доктор Вудроу, директор Аризонского Университета Диетологии подали иск в суд на FDA с возражением против одобрения аспартама, основываясь на нерешенных вопросах его безопасности.
Сентябрь 1983 – председатель FDA Артур Хейс под градом критики уходит в отставку. Причина – несанкционированные полеты на самолете, принадлежащем General Foods, крупнейшему потребителю NutraSweet. Burson-Marsteller, компания, занимающаяся связями с общественностью для Searle, а также предоставляющая такие услуги для некоторых крупных потребителей NutraSweet, немедленно наняла Хейса на должность главного научного консультанта.
Осень 1983 – первые газированные напитки, содержащие аспартам, вышли в розничную продажу.
Ноябрь 1984 - Центр по контролю и профилактике заболеваний (CDC) "Оценка жалоб потребителей, связанных с употреблением аспартама." (Краткое изложение Б. Mullarkey)
3 ноября 1987 - слушания США, "NutraSweet: Здоровье и обеспокоенность по поводу безопасности" Комитет по труду и кадрам, сенатор Говард Metzenbaum, председатель.</quote>
Весна 1967 - G.D. Searle начало тестирование аспартама на безопасность, требующееся для признания его годным к употреблению в пищу.
Осень 1967 – доктор Гарольд Вайсман, биохимик Университета Висконсина, по заказу G.D. Searle провел тесты аспартама на молодых обезьянах. Из семи обезьян, которые принимали аспартам, растворенный в молоке, одна умерла и ещё пять заболели тяжёлой формой эпилепсии.
Ноябрь 1970 – Цикламат, широко распространенный низкокалорийный синтетический подсластитель, был выкинут с рынка после того, как некоторые ученые связали его с возникновением рака. Вопросы возникли так же к Сахарину, второму синтетическому подсластителю на рынке, открывая аспартаму широкое поле для деятельности.
18 декабря 1970 – руководство G.D. Searle рассказало в своей стратегии о предчувствиях, что FDA «думает в положительном ключе об аспартаме». Внутренние документы описывали психологическую тактику, которая должна использовать компания, чтобы «FDA подсознательно прониклось духом сотрудничества и у руководства Управления вошло в привычку говорить «да».
Весна 1971 – нейробиолог Джон Олни (чьи работы о глутамате натрия ранее привели к удалению вещества из детского питания) информировал G.D. Searle, что аспарагиновая кислота, один из ингредиентов аспартама, в его опытах вызвала разрушение головного мозга у мышей. Один из сотрудников компании подтвердил результаты Олни в похожем исследовании.
Февраль 1973 – потратив десятки миллионов долларов на проведение тестирования, G.D. Searle подала заявку FDA на разрешение и приложила более сотни положительных исследований, доказывающих безопасность аспартама.
5 марта 1973 – один из ведущих ученых FDA в аннотации к тестам аспартама заметила, что приведенной G.D. Searle информации недостаточно, чтобы оценить потенциальную токсичность аспартама, и нужны дальнейшие клинические испытания.
Май 1974 – адвокат Джим Тернер (защитник прав потребителей, сыгравший роль в выведении Цикламата с рынка) встретился с представителями G.D. Searle по поводу исследования Джоном Олни аспарагиновой кислоты в 1971 году.
26 июля 1974 – FDA разрешило аспартам к ограниченному использованию в сухом питании.
Август 1974 – Джим Тернер и Джон Олни предоставили доказательства против аспартама.
24 марта 1976 – петиция Тернера и Олни возбудила расследование FDA лабораторной практики производителя аспартама G.D. Searle. Комиссия обнаружила в процедурах G.D. Searle большое количество несоответствий и манипулирования данными.
10 января 1977 – FDA сделало официальный запрос прокурору штата начать расследование против G.D. Searle за намеренное искажение данных, «сокрытие существенных фактов и дачу ложных показаний» в тестах безопасности аспартама. В первый раз в своей истории Управление по санитарному надзору возбудило уголовное дело на производителя.
26 января 1977 – во время расследования дела компания Sidley & Austin, юридическая фирма, представлявшая интересы G.D. Searle, начала переговоры с Самуэлем Скиннером, прокурором, ведущим расследование.
8 марта 1977 - G.D. Searle наняла на должность генерального директора видного вашингтонского политика Дональда Рамсфельда, который должен был помочь компании выйти из тяжелой ситуации. Бывший сенатор и Министр Обороны в администрации Форда, Рамсфельд привел с собой в высшее руководство компании нескольких своих помощников.
1 июля 1977 – Самуэль Скиннер, расследовавший дело G.D. Searle, покинул своё кресло и перешел на работу в Sidley & Austin.
1 августа 1977 – выпущено заключение Бресслера, составленное комиссией FDA под руководством Джерома Бресслера. Комиссия нашла, что во время тестирования 98 из 196 животных умерли и не были вовремя вскрыты, а некоторые тела ждали своей очереди более года. Также была отмечена масса других нарушений, например крыса по документам была живой, потом мертвой, потом снова живой и снова мертвой. У животных находили маточные полипы и злокачественные образования яичников, но это никак не отражалось в официальных отчетах G.D. Searle.
8 декабря 1977 – отставка прокурора Скиннера так затянуло следствие, что временное ограничение на выпуск аспартама потеряло свою силу. Уголовное дело было закрыто.
1 июня 1979 – FDA создает Общественный Совет по расследованию вопросов, связанных с безопасностью NutraSweet, торговой марки аспартама.
30 сентября 1980 – общественный совет постановил запретить NutraSweet к употреблению до проведения дальнейших исследований, связанных с опухолями мозга у подопытных животных. Совет утвердил, что не было предоставлено достаточных доказательств, что аспартам безопасен для использования в качестве пищевой добавки.
Январь 1981 – Дональд Рамсфельд, гендиректор G. D. Searle, заявил, что сделает всё возможное для разрешения аспартама к использованию в течение года, а также, что он будет использовать свой политический вес в Вашингтоне, а не научные средства, чтобы убедиться в принятии разрешения.
21 января 1981 – инаугурация Рональда Рейгана в качестве президента США. Команда Рейгана, в которую входит Дональд Рамсфельд, ставит на должность руководителя FDA Артура Халла Хейса.
Март 1981 – собрана комиссия FDA для рассмотрения вопросов, поднятых Общественным Советом по расследованиям.
19 мая 1981 – три из шести штатных биологов FDA, ответственных за рассмотрение случаев опухолей головного мозга животных, выступили против нового разрешения NutraSweet, основываясь на записях, что тестирование Searle было некачественным и недостаточным для признания аспартама безопасным.
15 июля 1981 – одним из своих первых приказов Артур Хейс, новый председатель FDA, действуя против указаний Общественного Совета и игнорируя рекомендации его собственной команды биологов разрешает NutraSweet к применению в сухом питании. Хейс сказал, что для предполагаемого применения аспартам доказал свою безопасность и лишь немногие вещества выдержали такое детальное тестирование и такое пристальное внимание.
15 октября 1982 – FDA анонсировало, что Searle прислало петицию о разрешении применения аспартама в газированных напитках и других жидкостях.
1 июля 1983 – Ассоциация Производителей Газированных Напитков (NSDA) попросила FDA отложить разрешение аспартама до проведения новых тестов, поскольку аспартам очень нестабилен в жидкой форме. Аспартам в жидкой форме при температуре выше 30 градусов Цельсия распадается на DKP (дикетопиперазины) и формальдегид – оба известные канцерогены.
8 июля 1983 - NSDA разработала возражения против принятия разрешения на использование аспартама в газированных напитках и сиропах и подала запрос на слушания по своим возражениям. NSDA сказала, что Searle не предоставила достаточно доказательств, что аспартам и продукты его разложения безопасны для использования в газированных напитках.
8 августа 1983 – защитник прав потребителей Джим Тернер из Национального Института Питания и доктор Вудроу, директор Аризонского Университета Диетологии подали иск в суд на FDA с возражением против одобрения аспартама, основываясь на нерешенных вопросах его безопасности.
Сентябрь 1983 – председатель FDA Артур Хейс под градом критики уходит в отставку. Причина – несанкционированные полеты на самолете, принадлежащем General Foods, крупнейшему потребителю NutraSweet. Burson-Marsteller, компания, занимающаяся связями с общественностью для Searle, а также предоставляющая такие услуги для некоторых крупных потребителей NutraSweet, немедленно наняла Хейса на должность главного научного консультанта.
Осень 1983 – первые газированные напитки, содержащие аспартам, вышли в розничную продажу.
Ноябрь 1984 - Центр по контролю и профилактике заболеваний (CDC) "Оценка жалоб потребителей, связанных с употреблением аспартама." (Краткое изложение Б. Mullarkey)
3 ноября 1987 - слушания США, "NutraSweet: Здоровье и обеспокоенность по поводу безопасности" Комитет по труду и кадрам, сенатор Говард Metzenbaum, председатель.</quote>
Оригинал: http://www.collective-evolution.com/2013/01/19/the-shocking-story-of-how-aspartame-became-legal/